Ne pas utiliser les gouttes pour les yeux du Dr Berne et LightEyez en raison de la présence de bactéries et de champignons, indique la FDA.
La FDA déconseille l'utilisation des gouttes pour les yeux du Dr Berne et LightEyez en raison de la présence de bactéries et de champignons.

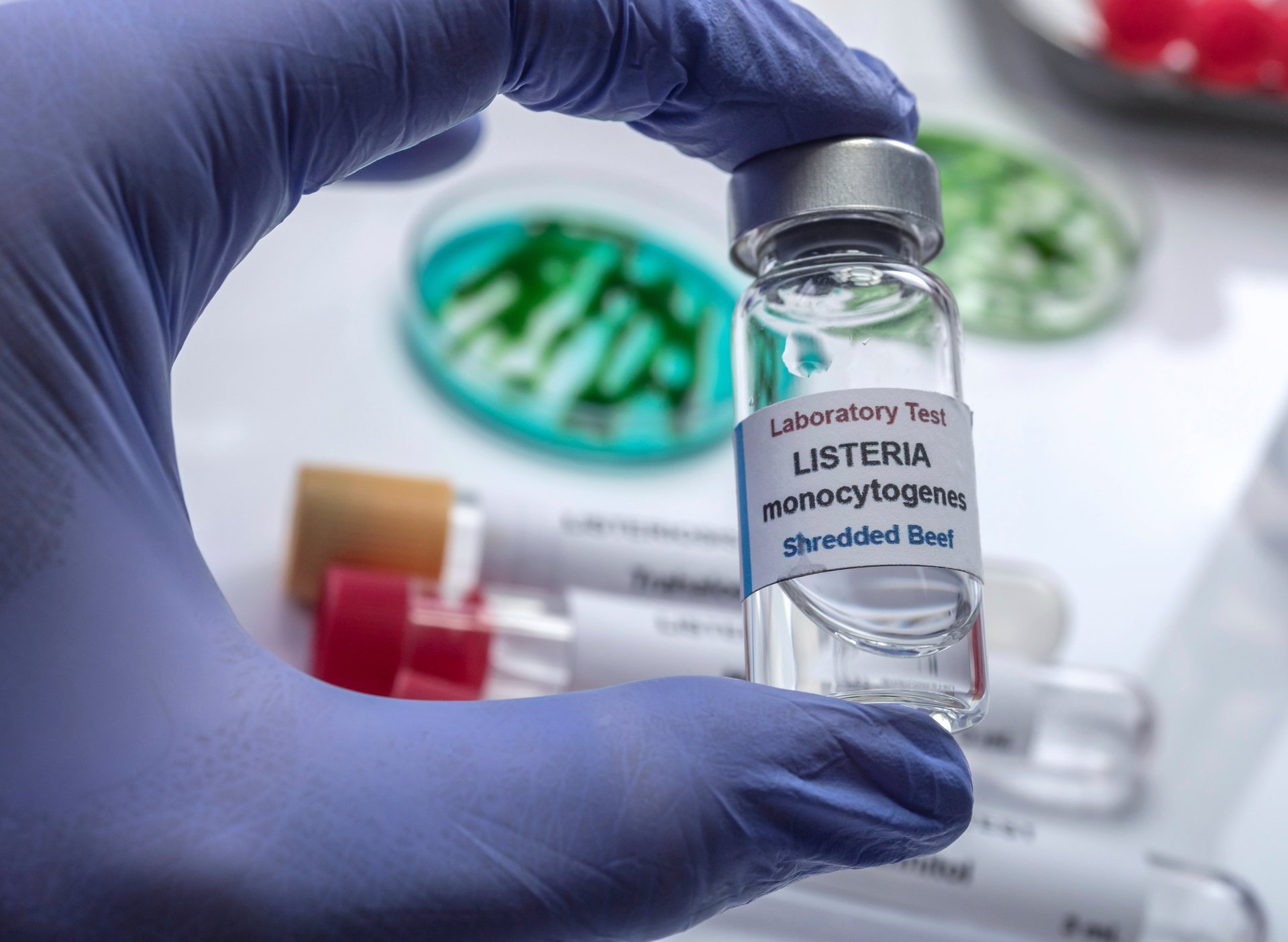
Des gouttes pour les yeux contaminées sont de retour dans les actualités, avec des avertissements des régulateurs fédéraux demandant aux consommateurs de ne pas utiliser certaines gouttes pour les yeux en raison de problèmes de contamination.
La Food and Drug Administration (FDA) des États-Unis a conseillé aux personnes d’éviter d’acheter et d’arrêter immédiatement d’utiliser la solution MSM Drops 5% du Dr. Berne et les gouttes pour les yeux LightEyez MSM Eye Drops—Eye Repair, car les gouttes peuvent être contaminées par des bactéries, des champignons ou les deux.
Les microbes spécifiques isolés lors des tests de la FDA comprennent Bacillus (une bactérie) et le champignon Exophiala dans la solution MSM Drops 5% du Dr. Berne.
Dans les gouttes pour les yeux LightEyez MSM Eye Drops—Eye Repair, les tests de la FDA ont détecté des bactéries, dont Pseudomonas, Mycobacterium, Mycolicibacterium et Methylorubrum.
- 1 mère américaine sur 5 déclare avoir été maltraitée lors des soins...
- Une autre source d’exposition au plomb pour les enfants la f...
- Les voyages spatiaux ont un impact sur le sang et les os des astron...
Les produits du Dr. Berne sont distribués par Dr. Berne’s Whole Health Products. Cette société a accepté lundi de rappeler volontairement ces gouttes pour les yeux spécifiques.
Les produits LightEyez sont distribués par LightEyez Limited. LightEyez n’a pas répondu à un courriel de la FDA demandant de discuter des préoccupations de l’agence.
Jusqu’à présent, personne n’a signalé d’événements indésirables liés à l’utilisation des gouttes, a déclaré la FDA, mais les produits doivent être jetés car leur utilisation peut entraîner des infections mineures ou graves menaçant la vision. Cela peut même évoluer vers une infection mettant la vie en danger, a averti l’agence.
Les patients présentant des signes ou des symptômes d’une infection oculaire doivent consulter leur professionnel de la santé ou demander des soins médicaux immédiats.
Les deux gouttes pour les yeux incluses dans l’avertissement contiennent également du méthylsulfonylméthane (MSM) en tant qu’ingrédient actif. Selon la FDA, aucun médicament ophtalmique légalement commercialisé ne contient du MSM en tant qu’ingrédient actif, donc ces produits sont des médicaments non approuvés et commercialisés illégalement aux États-Unis.
Les gouttes pour les yeux doivent être stériles selon la loi fédérale pour être sûres à utiliser. La FDA a déclaré avoir échantillonné et testé ces produits en raison des problèmes récents de fabrication de gouttes pour les yeux dans l’industrie des gouttes pour les yeux.
D’ici la fin mai de cette année, un total de 81 cas d’infections graves – liées à 10 marques de gouttes pour les yeux contaminées par une souche rare de bactéries résistantes aux médicaments – ont été signalés aux États-Unis.
Au total, quatre personnes sont décédées, selon les Centers for Disease Control and Prevention (CDC) des États-Unis, et un total de 14 personnes ont subi une perte de vision. Quatre cas concernaient des personnes atteintes d’infections si graves qu’elles ont dû se faire enlever chirurgicalement leurs globes oculaires.
L’épidémie signalée ce printemps concernait 10 marques de gouttes pour les yeux, le plus souvent EzriCare Artificial Tears. Les gouttes étaient distribuées par EzriCare et Delsam Pharma.
SOURCE : Food and Drug Administration des États-Unis, le 22 août 2023